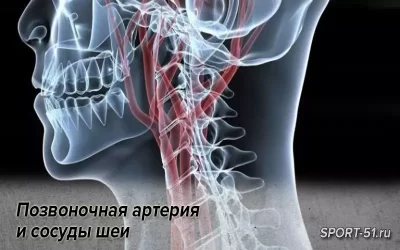
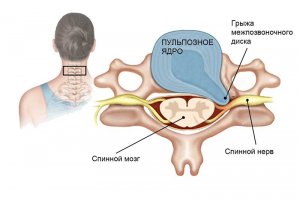
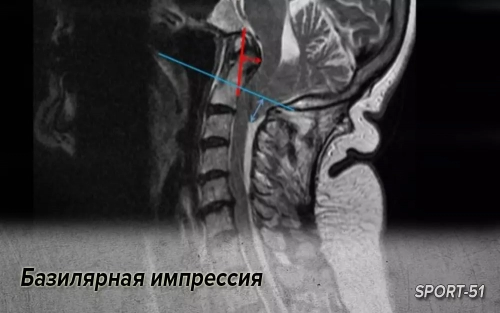
 Актуальность проблемы. Краниовертебральная область (КВО), представляя собой подвижную структуру шейного отдела позвоночника, одновременно является его наиболее ранимой зоной. Клинические проявления при повреждении КВО многообразны. В патологический процесс максимально включаются позвоночная артерия и сопровождающие ее нервные образования, которые и формируют основное патогенетическое ядро заболевания.
Актуальность проблемы. Краниовертебральная область (КВО), представляя собой подвижную структуру шейного отдела позвоночника, одновременно является его наиболее ранимой зоной. Клинические проявления при повреждении КВО многообразны. В патологический процесс максимально включаются позвоночная артерия и сопровождающие ее нервные образования, которые и формируют основное патогенетическое ядро заболевания.
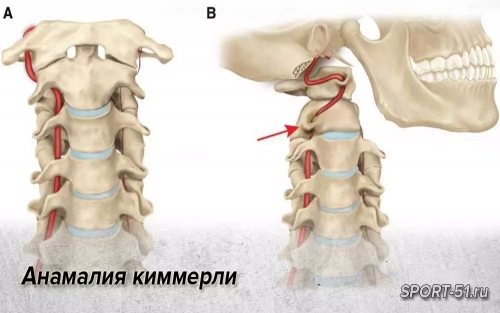
Одной из часто встречающихся аномалий КВО является костная перемычка, описанная в 1923 г. H. Hayek. Она располагается между задним краем суставного отростка атланта и задней границей его дуги и формирует отверстие, через которое проходят позвоночная артерия (ПА) и затылочный нерв. Более детально данная патология была описана в 1930 г. венгерским врачом А. Киммерле, обратившим внимание на то, что данное изменение может приводить к расстройствам мозгового кровообращения, и впоследствие получила его имя – аномалия Киммерле (АК).
В основе развития этой костной патологии лежит несоответствие нервных элементов спинного мозга и позвоночных тканей. К ним относятся окципитализация атланта либо остатки протоатланта с прогредиентным ростом, постепенным обызвествлением атлантозатылочной мембраны при микроповреждениях или микрокровоизлияниях, полученных во время травм КВО. В результате этих изменений ПА проходит не в борозде дуги атланта, а в отверстии, образованном с одной стороны бороздой, а с другой – оссифицированной атлантоокципитальной связкой, формирующей своеобразный костный мостик. Он ограничивает свободный ход ПА и затылочного нерва при движении головы, особенно при ее поворотах.
А.А. Луцик (1988) придает первостепенное значение рубцовому перерождению стенки артерии и периартериальной клетчатки вследствие длительной травматизации ПА в области АК, что приводит к развитию повреждения интимы, раннему формированию атеросклеротических бляшек, суживающих просвет сосуда, и/или диссекций. В результате резкие движения головы могут провоцировать процесс дестабилизации гемодинамики пораженной артерии и превращаться в источник нарушений кровоснабжения дистальных отделов вертебрально-базилярной системы (ВБС) по механизму Bow Hunter Stroke.
 Таким образом, патогенез расстройств гемодинамики в ВБС при АК этиологически обусловлен развитием сложного компрессионно-стенозирующего ирритативного эффекта, вследствие чего наблюдается снижение объемного кровотока по ПА, развитие недостаточности кровообращения в той или иной степени в ВБС.
Таким образом, патогенез расстройств гемодинамики в ВБС при АК этиологически обусловлен развитием сложного компрессионно-стенозирующего ирритативного эффекта, вследствие чего наблюдается снижение объемного кровотока по ПА, развитие недостаточности кровообращения в той или иной степени в ВБС.
При анатомических исследованиях различные варианты АК выявляются примерно у 30% населения. У больных с клиникой вертебробазилярной дисфункции (кохлео-вестибулярные расстройства, атаксия, зрительные нарушения и др.) или с миофасциальными болями по типу синдрома Тонзика АК обнаруживается в 7,6% случаев. Мостик бывает неполным, одно- или двухсторонним, поэтому различают разные степени этой аномалии. Следует отметить, что толщина мостика и величина отверстия также значительно варьируют.
Клиническая картина начальных проявлений АК характеризуется многообразием симптоматики (головокружение, вегетативные дисфункции, головные боли, преходящие изменения зрения, боли в шее), что создает трудности в определении распространенности начальных проявлений АК, которые обусловлены тем фактом, что периодически возникающую головную боль на начальных этапах патологии пациенты, а зачастую и врачи не относят к серьезным заболеваниям. Таким образом, они длительное время наблюдаются с различными диагнозами, такими как «мигрень», «цефалгия», «головная боль напряжения», «ВСД» и т.д. у разных специалистов, получают разнородное обследование и лечение, что в результате не позволяет сформировать необходимую статистическую базу.
В развернутой стадии, развивающейся в 20% всех случаев АК, в клинической картине заболевания преобладают симптомы ишемии структур, питаемых ВБС, такие как начальные проявления недостаточности мозгового кровообращения (НПНМК) и/или пароксизмальные нарушения мозгового кровообращения (ПНМК). НПНМК проявляются в виде головокружений, нарушений слуха, шума, звона в ушах, головной боли в области затылка, ощущений «точек или песка» перед глазами, иногда цветных фотопсий.
 В межприступный период больные жалуются на пелену перед глазами, давление в наружном слуховом проходе, шум, гиперакузию, утомляемость, нарушение сна. Очаговая неврологическая симптоматика отсутствует. Четко прослеживается зависимость каждого из симптомов от перемещения тела в пространстве.
В межприступный период больные жалуются на пелену перед глазами, давление в наружном слуховом проходе, шум, гиперакузию, утомляемость, нарушение сна. Очаговая неврологическая симптоматика отсутствует. Четко прослеживается зависимость каждого из симптомов от перемещения тела в пространстве.
ПНМК характеризуются более выраженными симптомами: приступообразно возникающие несистемные головокружения, часто с тошнотой, рвотой (при разгибании и поворотах головы); нарушения слуха (шум, звон в ушах); головные боли (преимущественно в затылочной области); зрительные нарушения (затуманенное зрение, фотопсии, дефекты полей зрения); патологические пирамидные знаки; расстройства чувствительности; мозжечковые и бульбарные симптомы; моно-, пара- или тетрапарезы; внезапные падения без потери сознания (drop-attacks); внезапные падения с потерей сознания (синкопальный синдром Унтерхарншейдта). Все симптомы ПНМК должны сохраняться не более 24 ч.
Наиболее выраженным осложнением нарушений кровообращения в ВБС является ишемический инсульт в системе ВББ, при котором формируются небольшие очаги размягчения в области мозжечка и продолговатого мозга, что клинически проявляется стойкой неврологической недостаточностью в виде общемозговых и очаговых неврологических симптомов, поражения срединно-стволовых и мозжечковых структур, которые сохраняются у пациентов более 24 ч.
Гуляев С.А., Кулагин В.Н., Архипенко И.В., Гуляева С.Е. (2013) провели исследование с целью анализа частоты встречаемости АК в структуре неврологического стационара, разработки критериев ее диагностики и рациональных методов терапии. В исследовании использовались результаты скринингового обследования пациентов, госпитализированных в неврологическую клинику ГОУ ВПО ВГМУ за период 6 лет (всего 8 436 человек).
Критерием исключения являлось наличие верифицированных черепно-мозговых травм и травм шейного отдела позвоночника, сосудистых аномалий, опухолей этой зоны. Комплекс обследований помимо клинико-неврологического включал рентгенографию позвоночника и черепа, КТ, МРТ головного и спинного мозга, ультразвуковое исследование сосудов шеи и головного мозга (УЗДГ, ДС), ЭЭГ. Все обследования проводились в динамике трехлетнего наблюдения с частотой от 2–х до 6 раз в год.
В ходе исследования было выявлено 68 больных с АК в возрасте от 18 до 67 лет, среди них 42 (61,8%) женщины и 26 (38,2%) мужчин. В большинстве случаев (74,6%) клинические проявления неврологического дефекта приобретали стабильность к 20 - 25 годам. Однако исследования анамнеза показали, что у 43,8% обследованных и ранее возникали специфические жалобы, свидетельствующие о наличии патологии КВО, которые расценивались специалистами как спастическая кривошея, цервикобрахиалгия, синкопальные состояния, гемоликвородинамические нарушения и др.
 Результаты исследования. Клиническая картина, выявленная у больных АК, характеризовалась многообразием симптоматики, но, учитывая ведущий клинический признак, было выделено 3 основных неврологических синдрома.
Результаты исследования. Клиническая картина, выявленная у больных АК, характеризовалась многообразием симптоматики, но, учитывая ведущий клинический признак, было выделено 3 основных неврологических синдрома.
- Болевой синдром, характеризовавшийся половинным характером головной боли с локализацией преимущественно в затылочной области (91,6% наблюдений) с иррадиацией в глаз или слуховой проход, сопровождавшийся в 43,9% случаев фотопсиями, выпадениями полей зрения (34,6%) или метаморфопсиями (21,5%).
- Синдром сосудистой недостаточности, проявлявшийся в 42,6% случаев в виде головокружения (79,4%), шаткости при ходьбе, нестойких нарушений координационных проб (61,7%), сопровождавшихся в 54,4% наблюдений тошнотой и рвотой. Реже больные отмечали появление шумовых иллюзий в виде жужжания, шуршания, писка, свиста, локализующихся то в ухе, то в голове (45,8%). Характерной особенностью данного синдрома была его связь с поворотами головы, проявляющаяся в его нарастании при совершении движения, что вынуждало пациентов занимать определенную позу (так называемая позиционность головы).
- Вегетативный синдром (синдром панических атак) регистрировался у 41,1% обследованных, отличался внезапным развитием с возникновением чувства «прилива жара» к голове или шее, сопровождался немотивированным страхом, тревогой, чувством удушья с ярко выраженными дисфункциями автономной неравной системы (ознобоподобное дрожание, онемение рук, нестабильность АД и др.). По окончании приступа у пациентов наблюдались полиурия и панастения. Их длительность колебалась от десятков минут до нескольких часов.
Наблюдение за пациентами в динамике позволило выявить три степени тяжести заболевания:
- I легкая – характеризовалась только наличием болевого синдрома в сочетании с гемо-ликворо-динамическими нарушениями;
- II средняя – к проявлениям первой степени присоединялись вегетативные дисфункции перманентного и пароксизмального характера с частотой пароксизмов 3–4 раза в год;
- III тяжелая – при ней частота основных синдромов колебалась от ежемесячных до еженедельных.
Катамнестический анализ показал прямую зависимость тяжести течения от длительности заболевания и возможность постепенной и прогредиентной трансформации клинических форм заболевания от легкой через среднюю (68,7±0,3%, p<0,05) до тяжелой (31,3±0,2%, p<0,05).
Лечение АК. Выбор тактики лечения клинических проявлений АК базировался на патогенетическом принципе, потому что этиологическое лечение требует проведения оперативного вмешательства не только на самом костном образовании кольца атланта, но и проведения реконструктивной ангиопластики позвоночной артерии, что не всегда целесообразно на ранних стадиях заболевания, представляющих большинство клинических случаев. Поэтому предпочтение в выборе схемы лечения было отдано терапевтическим методам.
Основная патогенетическая модель базировалась на принципах «порочного круга», в основе которого находится раздражение затылочного нерва, приводящее к возникновению болевого синдрома и защитного напряжения мышц шеи и скальпа. В свою очередь, формирующаяся миотония приводит к нарушению нормальных биомеханических соотношений, что вызывает еще большее раздражение затылочного нерва и соответствующую прогрессию боли с присоединением вегетативных нарушений из-за раздражения нерва Франка и сопровождающих позвоночную артерию сплетений, а также синдромов недостаточности кровоснабжения ВБС на более поздних этапах.
В основу терапевтического воздействия на данную патогенетическую модель были положены методы, позволяющие купировать болевой синдром, редуцировать миотонические симптомы и улучшить трофику сосудистых и нервных структур. В качестве базовых медикаментозных средств использовались нестероидные противовоспалительные препараты быстрого действия (лорноксикам и др.), миорелаксанты периферического действия (толперизон), комплексные витаминосодержащие препараты трофического и анаболического действия.
Дополнительно в курс лечения включались лечебная физкультура, массаж. Лорноксикам, назначаемый для купирования болевого синдрома, был эффективен у всех пациентов. Кардиальные дисфункции, нарушения функций ЖКТ преобладали у пациентов старшей возрастной группы. Таким образом, исходя из полученных данных, НПВП лорноксикам показал себя как высокоэффективное обезболивающее средство у пациентов всех возрастных групп, однако из-за быстрого развития побочных эффектов препарат лучше назначать однократно для экстренного купирования болевого синдрома.
Обсуждение и выводы. Оссификация атлантоокципитальной связки представляет собой нередкий вариант аномалии строения КВО. Данная аномалия встречается практически во всех возрастных группах с максимальной представленностью в возрасте 25 лет и старше. В клинической картине заболевания преобладают три основных синдрома: болевой синдром, синдром сосудистой недостаточности и синдром вегетативных дисфункций.
Тяжесть клинических проявлений соответствует трем степеням, отражающим разные типы течения, – легкой, среднетяжелой и тяжелой, характеризуется частотой обострений и зависит от выраженности анатомического дефекта. Тесное расположение различных элементов, а также сочетание разных патологических процессов, развивающихся в шейном отделе позвоночника, в большинстве случаев затрудняет активные хирургические вмешательства, что требует разработки консервативных методов лечения, направленных на купирование болевого синдрома, редуцирование миотонического напряжения мышц шеи и скальпа, а также активацию репаративных процессов в пораженной зоне.
Использование обезболивающих препаратов группы оксикамов, в частности лорноксикама, высокоэффективно у пациентов с АК в качестве экстренной помощи при развитии болевого синдрома в однократном применении. При необходимости более длительного использования данного препарата необходимо проводить защитные меры по профилактике поражения структур ЖКТ.
Также препарат следует назначать с осторожностью лицам старших возрастных групп из-за риска развития кардиальной патологии. Применение в схеме лечения препаратов миорелаксирующего и репаративного (витаминного) действия позволяет эффективно убрать основные клинические проявления АК и ввести заболевание в состояние ремиссии на период до 9 месяцев.